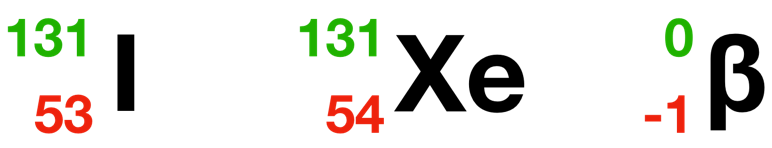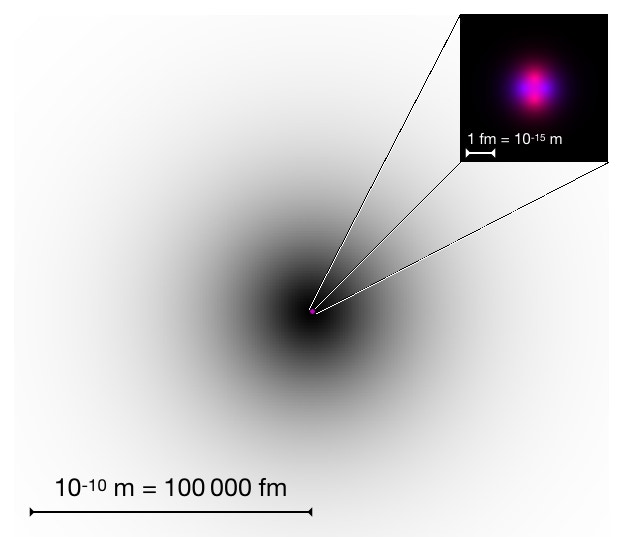
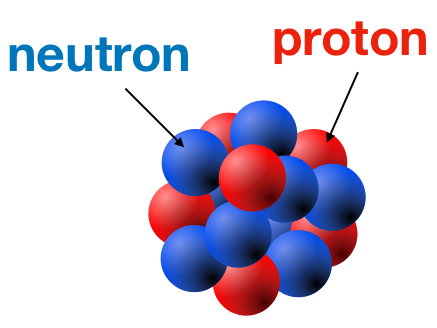
Notation symbolique d’un élément :
- • X est le symbole chimique de l’élément (C, Na, Cu, par exemple)
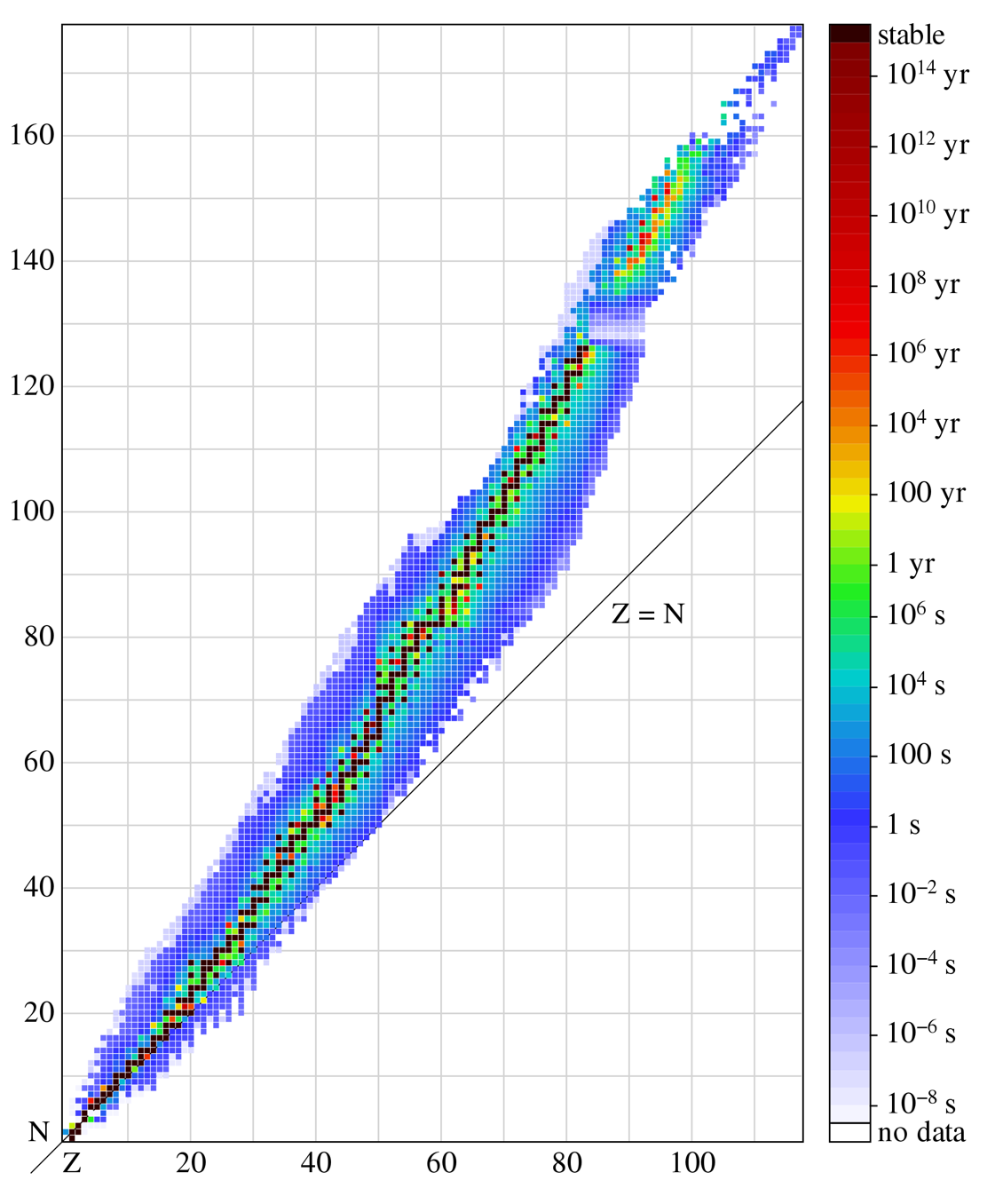
- • Z est le numéro atomique : c’est le nombre de protons du noyau.
- • Pour chaque Z correspond un symbole X et un seul (1 → H, 2 → He, 3 → Li, etc.)
- • A est le nombre de masse ou nombre de nucléons (protons + neutrons)
du noyau.
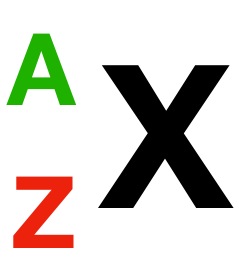
Le nombre de neutrons N d’un noyau vaut donc :
😒
N = A
OUI
N = A − Z
😞
N = A + Z