Exemple de la pile Daniell :
La réaction d’oxydoréduction d’une pile
est spontanée = elle libère de l’énergie.

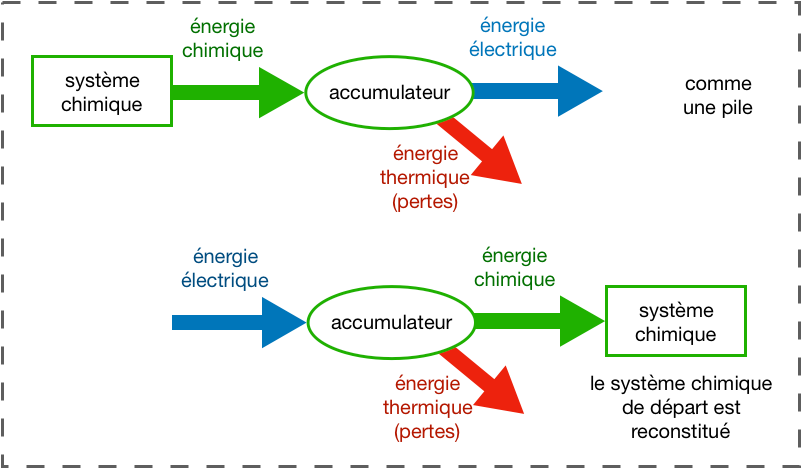
On peut forcer la réaction
inverse, appelée électrolyse,
pour recharger le dispositif.
On ne parle alors plus de piles
mais d’accumulateurs pour ces systèmes réversibles.
La quantité d’électricité disponible, ou capacité électrique Q de la pile (en coulomb C), vaut :

- ne est la quantité d’électrons échangés dans la pile (en mol)
- F (Faraday) est la valeur absolue de la charge d’une mole d’électron (1 F = 9,65.104 C.mol-1)
Si la pile débite un courant d’intensité I (en A), elle va se vider en une durée Δt donnée par :
La capacité électrique d’une pile est souvent notée en A.h par les fabriquants.
À combien de coulomb correspond 1 A.h ?
La caractéristique d’une pile (U,I) est donnée par la formule U = E - r×I,
où E (en V) est la tension à vide de la pile (sans courant), appelée force électromotrice f.e.m., et r (en Ω) est la résistance interne de la pile, responsable des pertes.

L’énergie disponible, ou charge énergétique W (en J), d’une pile vaut alors :

L’énergie massique des batteries (ensemble d’accumulateurs)
des voitures électriques et hybrides est aujourd’hui
supérieure à 100 Wh/kg.

Exemple : quelle est l’énergie contenue dans cet accumulateur ?
