Un liquide est un état condensé : les molécules s’attirent. Lorsque cette attraction l’emporte sur l’agitaton thermique, les molécules passent d’une phase gazeuse à une phase dense mais encore désordonnée : un liquide. Les molécules au sein du liquide bénéficient d’interactions attractives avec toutes leurs voisines et sont dans un état « heureux ». Au contraire, à la surface du liquide, elles perdent la moitié des interactions cohésives et sont « malheureuses ». C’est pour cette raison que les liquides vont ajuster leur forme pour exposer le minimum de surface : vos cheveux secs sont bouffants et volumineux, mais une fois mouillés, ils collent ensemble tristement.
Exposé à la surface, une molécule est donc dans un état énergétique défavorable. Si U est l’énergie de cohésion par molécule, une molécule à la surface perd en gros ½U. La tension de surface mesure directement ce défaut d’énergie par unité de surface. Si a est la dimension moléculaire et a² la surface exposée par molécule, la tension de surface est γ ∼ U/(2a²). Plus les interactions attractives sont fortes, plus la tension de surface est grande. Pour la plupart des huiles, où les interactions sont de type van der Waals, U est de l’ordre de grandeur de l’agitation thermique : U ∼ kBT. À 25°C, kBT vaut 1/40 eV, ce qui donne : γ ∼ 20 mJ/m². Pour l’eau, à cause des liaisons hydrogènes, γ est plus grand (γ ∼ 72 mJ/m²). Pour le mercure, qui est un métal liquide très cohésif, U ∼ 1 eV et γ ∼ 500 mJ/m².
Extrait de «Gouttes, bulles, perles et ondes»
de Pierre-Gilles de Gennes et al.
γ est l’énergie à fournir pour augmenter la surface d’une unité mais elle peut aussi être considérée comme une force
par unité de longueur
(1 mJ/m² = 1 mN/m)
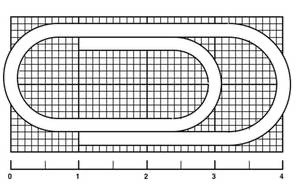
dimensions
(le quadrillage est millimétré)
et masse : m = 1,1 g
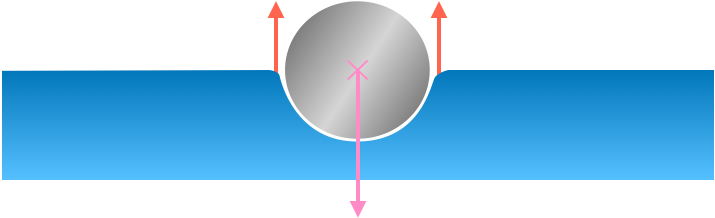
À partir de l’expérience du trombone dont les caractéristiques sont reportées ci-dessus, estimez une borne inférieure à la tension superficielle γ de l’eau. Commenter/critiquer.
Du liquide vaisselle a été déposée sur la pointe du couteau. On observe, dans un premier temps, que le trombone « fuit » le couteau, c’est l’effet Marangoni, puis le trombone coule.
Que peut-on dire maintenant de la tension superficielle ?
Explication microscopique ?